- This Project has received funding from the European Union´s Horizon 2020 research and innovation programme under grant agreement No 945118
- Inicio
- El ProyectoEl Proyecto de RESILIENCE
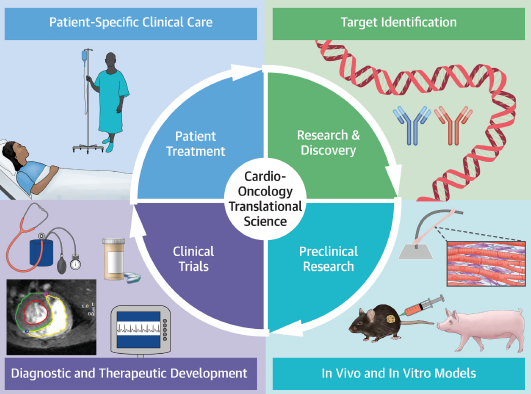
El proyecto RESILIENCE desarrolla una intervención destinada a reducir la prevalencia de insuficiencia cardíaca crónica en pacientes que hayan superado un cáncer. Se trata del condicionamiento isquémico remoto, conocido por su abreviatura en inglés como RIC (Remote Ischemic Conditioning). El objetivo buscado con este procedimiento es una reducción en la incidencia de la insuficiencia cardíaca en los pacientes que han superado un cáncer y que han recibido tratamiento quimioterápico con potencial efecto dañino a nivel del corazón.
Reducir la insuficiencia cardíaca en pacientes que hayan superado un cáncerSegún la OMS, se espera que la incidencia de cáncer aumente en un 70% en los próximos 20 años. La mitad de las personas diagnosticadas con cáncer sobrevivirán durante al menos una década tras el mismo, y se espera que esta tasa de supervivencia aumente significativamente en el futuro.
El condicionamiento isquémico remotoEl condicionamiento isquémico remoto (RIC) es un fenómeno por el cual episodios breves y repetidos de interrupción de la circulación en un miembro (brazo) favorecen el envío de señales a otros órganos como por ejemplo al corazón, y los hace así más resistente a posibles daños. En este caso, más resistentes a la posibilidad del daño cardíaco por la quimioterapia.
Consorcio multidisciplinarSe trata de una colaboración multidisciplinar en la que contamos con el apoyo de la industria, los científicos, los profesionales sanitarios como médicos y enfermeras, y de los propios pacientes implicados.
- Resonancia magnética cardiaca
La resonancia magnética cardíaca (RMC) es una prueba de imagen en la que los pacientes no reciben radiación. Se considera la prueba más precisa para la evaluación de la forma, función y composición de los tejidos del corazón.
El ensayo RESILIENCE utilizará la RMC como la principal herramienta para evaluar los resultados de la terapia de condicionamiento remoto, y los pacientes se someterán a un total de 3 exploraciones con la misma durante el estudio.



- Ensayo clínico
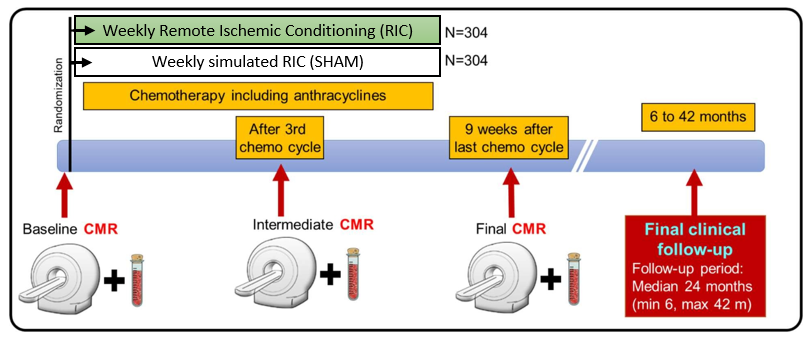
Se trata de un ensayo clínico multicéntrico, prospectivo, de fase II, aleatorizado, doble ciego con control simulado(placebo) para evaluar la eficacia y la seguridad del condicionamiento isquémico remoto (RIC) en pacientes con linfoma que vayan a recibir tratamiento quimioterápico con antraciclinas (al menos 5 ciclos).

- Pacientes
- Actualidad4 diciembre 2023
- Blog